PRACTICA 7: JUEGO DE COLORES.
INTEGRANTES DEL EQUIPO
PIRY HERRERA JASSO
-3cpiryherreraj16.blogspot.mx
KEVIN EDUARDO JIMENEZ ROMO
-3ckevinjimenezr.blogspot.mx
LEGNA CAROLINA LIRA AGUILA
-3clegnaliraA18.blogspot.mx
BRISSA ARANDEY LOPEZ REYES
-3cbrissalopezr19blogspot.mx
KATIA DEYANIRA LOPEZ SERNA
-3cKatiaLopezs20.blogspot.mx
GUILLERMO AXEL MACIAS MACIAS
-
FECHA DE EALIZCION:MIERCOLES 16 DE DICIEMBRE DE 2015
OBJETIVO:
PIRY HERRERA JASSO
-3cpiryherreraj16.blogspot.mx
KEVIN EDUARDO JIMENEZ ROMO
-3ckevinjimenezr.blogspot.mx
LEGNA CAROLINA LIRA AGUILA
-3clegnaliraA18.blogspot.mx
BRISSA ARANDEY LOPEZ REYES
-3cbrissalopezr19blogspot.mx
KATIA DEYANIRA LOPEZ SERNA
-3cKatiaLopezs20.blogspot.mx
GUILLERMO AXEL MACIAS MACIAS
-
FECHA DE EALIZCION:MIERCOLES 16 DE DICIEMBRE DE 2015
Identificación de elementos mediante el color de la flama.
HIPOTESIS:
Pensamos que el color de la flama cambiaria a una tonalidad parecida a la sustancia original.
Creímos que la flama se quedaría del color de la sustancia un momento después de quitar el grafito con esta.
INVESTIGACIÓN:
¿Que es el espectro de emisión atómica? Investiga la composición de los fuegos pirotécnicos.
Modelos de Lewis para los compuestos químicos de la practica.
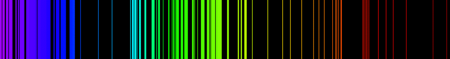
ESPECTRO DE EMISION
El espectro de emisión atómica de un elemento es un conjunto de frecuencias de las ondas electromagnéticas emitidas por átomos de ese elemento, en estado gaseoso, cuando se le comunica energía. El espectro de emisión de cada elemento es único y puede ser usado para determinar si ese elemento es parte de un compuesto desconocido.
Modelos de Lewis para los compuestos químicos de la practica.
ESPECTRO DE EMISION
El espectro de emisión atómica de un elemento es un conjunto de frecuencias de las ondas electromagnéticas emitidas por átomos de ese elemento, en estado gaseoso, cuando se le comunica energía. El espectro de emisión de cada elemento es único y puede ser usado para determinar si ese elemento es parte de un compuesto desconocido.
Las características del espectro de emisión en algunos elementos es claramente visible cuando estos elementos son calentados. Por ejemplo, cuando un alambre de platino es bañado en una solución de nitrato de estroncio y después es introducido en una llama, los átomos de estroncio emiten color rojo. De manera similar, cuando el Cobre es introducido en una llama, ésta emitirá una luz verde. Estas caracterizaciones permiten identificar los elementos mediante su espectro de emisión atómica.
COMPOCISION DE LOS FUEGOS PIROTECNICOS
MATERIAS PRIMAS
DIAGRAMAS DE LEWIS
1.-H2O
2.-LiCl

3.-NaCl
4.-KCl
5.-BaCl2
6.-SrCl2
7.-CuS

8.-CoCl3
Libreta de apuntes
MATERIAL:
- Mechero de bunsen.
- Vidrio de reloj.
- Barra de grafito gruesa.
- Lentes.
SUSTANCIAS:
- Agua
- Cloruro o sulfato de litio.
- Cloruro de sodio.
- Cloruro de potasio.
- Cloruro de bario.
- Cloruro de estroncio.
- Sulfato de cobre (II).
PROCEDIMIENTO EXPERIMENTAL:
Encendimos el mechero .La maestra iba pasando con determinada sustancia nosotros teníamos que introducir el grafito del lápiz en el agua que contenía el vidrio de reloj y luego en la sustancia, una vez que el grafito tenia la sustancia lo poníamos en la flama del mechero para observar el cambio de color en la flama una vez que lo observábamos limpiábamos el grafito y repetíamos el proceso con cada sustancia.
PROTOCOLO DE SEGURIDAD
Usar los lentes de protección hasta el final de la practica
Cuidar el vidrio de reloj para evitar romperlo
No dejar mucho tiempo el grafito del lápiz sobre la flama del mechero.
PROCEDIMIENTO:
- Coloca una cantidad pequeña de agua en el vidrio de reloj. (Nota: maneja el ácido con mucho cuidado, pues es muy corrosivo)
- Anota el color original de las sustancias y completa el cuadro.
SUSTANCIA
|
COLOR ORIGINAL (PROPIEDADES INTENSIVAS)
|
COLORACIÓN DE LA FLAMA
|
| Cloruro de litio LiCl | Viscoso | Rosa mexicano |
| Cloruro de sodio NaCl |
Duro, Cristalino
| Naranja |
| Cloruro de potasio KCl | Poco tenaz | Rosa |
| Cloruro de estroncio SrCl2 | Duro | Rojo |
| Cloruro de cobalto CoCl3 | Poroso | Amarillo como chispas |
| Sulfato de cobre CuSo4 | Duro, Poroso | Verde acua |
- Humedece la punta del grafito con el agua.
- Toma un poco de la primera sustancia con la punta del alambre o grafito. Acércala a la flama del mechero.
- Observa detenidamente el color que presenta la flama y anótalo en el cuadro.
- Introduce el grafito en el agua para limpiarlo y humedecerlo nuevamente.
- Repite la prueba de coloración a la flama con el resto de las sustancias.
OBSERVACIONES (IMÁGENES Y DESCRIPCIÓN):
El agua en el vidrio de reloj
Los lápices que utilizamos.
Cloruro de litio
Cloruro de sodio
cloruro de potasio
Cloruro de estroncio
Cloruro de cobalto
Sulfato de cobre
CONCLUSIÓN:
Nosotros al ver la flama observamos que el color de la sustancia no influye en el color resultante de la flama sino que cada sustancia varia el tono de la flama según sus electrones de valencia ya que las sustancias buscan ser estables por esto el cambio de color.
Los colores que se deben obtener son los siguientes:
cloruro de litio-carmín
cloruro de sodio-amarillo
cloruro de potasio-violeta pálido
cloruro de estroncio-escarlata
cloruro de cobalto-Fuegos artificiales
sulfato de cobre-verde esmeralda
https://l.facebook.com/l.php?u=http%3A%2F%2Fwww.quimitube.com%2Fensayos-de-coloracion-a-la-llama-para-l...%26nbsp&h=TAQFNhsuO















Calificación 10
ResponderBorrardisculpen no entendi muy bien para el color esmeralda me podrian decir que sales y metal usan
ResponderBorrar